La majorité des produits alimentaires font apparaitre de l’huile et de l’eau dans leur composition. La nature chimique de ces deux composés est tellement différente qu’il est bien connu de tous qu’aucun mélange n’est possible. Pour autant, la cohabitation entre l’huile et l’eau au sein d’un même volume doit pouvoir se faire. Pour faire coexister l’huile et l’eau de manière durable, il faut en savoir plus dans le domaine des émulsions mais entre les systèmes simples, multiples, directs, inverses, de Pickering…il est parfois difficile de s’y retrouver. Posons donc les bases.
1- Le sens de l’émulsion
La définition même d’une émulsion est qu’une phase est dispersée sous la forme de gouttelettes dans une autre, de nature différente. La phase qui se trouve la forme de gouttelettes est appelée la « phase dispersée » tandis que l’autre est appelée la « phase continue ». Selon si l’huile ou l’eau constitue la phase dispersée, la typologie et l’appellation même de l’émulsion sera différente. On retrouve alors principalement deux sortes :
- Emulsion directe : La phase huile se retrouve dispersée dans la phase aqueuse. On appelle cela des émulsions Huile-dans-Eau et on le note H/E. La plupart des produits alimentaires sont constitués comme cela : mayonnaise, pâtes céréalières, lait & crèmes…
- Emulsion inverse : La phase aqueuse se retrouve dispersée dans l’huile. De la même manière on appelle cela les émulsions Eau-dans-Huile, E/H. Ici, les applications sont plus restreintes mais le beurre ou la margarine sont des produits connus qui font apparaitre cette configuration.
Il existe également ce que l’on appelle les émulsions multiples à savoir par exemple qu’une phase est emprisonnée dans une seconde de nature différente et le tout se retrouve sous la forme de gouttelettes dans une troisième phase identique à la première. Typiquement on parle d’émulsions Eau-dans-Huile-dans-Eau (E/H/E). Il n’existe pas d’exemples concrets à ce jour mais la recherche en alimentaire reste intéressée par cette typologie d’émulsion car cela permet de conserver une configuration d’émulsion directe tout en ayant de l’eau au cœur des globules d’huile, l’intérêt étant alors d’alléger en matière grasse dans dénaturer le gout premier des aliments.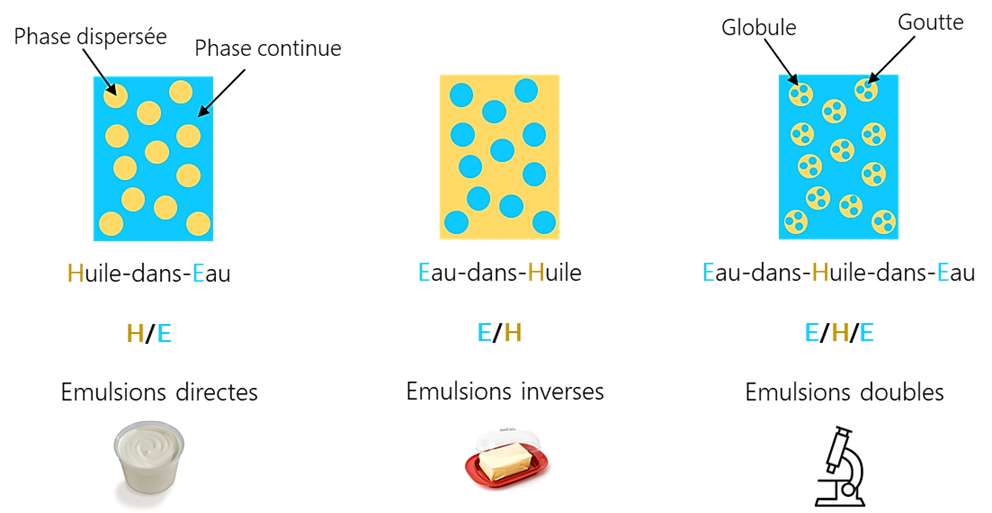
Pour dicter le sens préférentiel des émulsions, on peut jouer sur la proportion des phases. Par exemple, si on met un large excès d’eau par rapport à l’huile, on peut parfois forcer le système à se retrouver majoritairement « direct » (sauf cas particuliers). Malgré tout, le sens de l’émulsion est surtout dicté par l’agent émulsifiant utilisé pour stabiliser l’ensemble.
2- La nature de l’interface
Pour maintenir l’état dispersé (gouttelettes dans un continuum de nature différente), les émulsions doivent être stabilisées par des agents émulsifiants. Ces composés, décrits spécifiquement dans un autre article, présentent la particularité d’avoir, au sein de leur molécule, une partie qui aime l’eau (hydrophile) et une autre qui aime l’huile (lipophile). Compte tenu de cette dualité, ces composés se placent spontanément au niveau de l’interface entre l’eau et l’huile et aident à protéger les gouttelettes de leur recombinaison (pour voir comment les émulsions se déstabilisent c’est par ici).
Plusieurs composés permettent de stabiliser les émulsions, Il est donc également possible de possible de catégoriser les natures d’émulsions selon la composition même de l’interface :
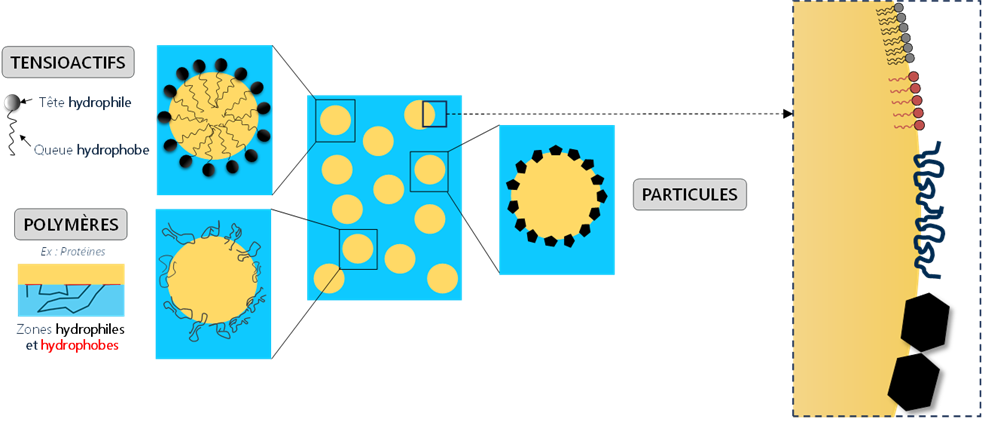
- Les émulsions « classiques » : généralement, ces émulsions sont stabilisées par des molécules dites tensioactives qui se schématisent par une tête (hydrophile) et une queue (lipophile). Le poids moléculaire de ces molécules est généralement faible. Par conséquent, ils se diffusent très vite aux interfaces, stabilisent rapidement et occupent peu d’espace. Parmi les émulsifiants les plus connus, on trouve la lécithine ou encore les mono- et diglycérides d’acides gras.
- Les émulsions protéiques : Les protéines sont constitués d’acides aminés dont leur enchainement permet d’obtenir une alternance de blocs hydrophiles et hydrophobes. Ainsi, leur structure confère des propriétés tensioactives. Les protéines, présentent un poids moléculaire plus important que précédemment ce qui fait que la migration à l’interface est plus lente. Le taux de couverture interfacial est plus important et l’avantage des protéines est qu’elles se déplient et stabilisent très bien les gouttelettes en formant une couche viscoélastique à la surface. Les protéines laitières sont couramment utilisées même si les protéines végétales sont de plus en plus utilisées aujourd’hui.
- Les émulsions de Pickering : Ces émulsions, qui portent le nom de celui qui les a découvert, sont très particulières et sont très étudiées aujourd’hui car elles représentent un challenge intéressant dans le domaine du clean-label et de l’économie circulaire. Il s’agit ici de stabiliser l’interface par des particules qui présentent des affinités intermédiaires entre l’eau et l’huile. Ces particules sont beaucoup plus lourdes que les agents présentés précédemment ce qui fait que leur diffusion aux interfaces peut être relativement faible. Cependant, lorsqu’elles s’adsorbent, l’ancrage est généralement irréversible. Les stabilités sont donc relativement longues. Parmi les plus étudiées on trouve les particules de cacao, les particules de curcuma ou le thé Matcha. Un aperçu global des particules alimentaires utilisées se trouve ici : https://www.annualreviews.org/content/journals/10.1146/annurev-food-081114-110822
 3- Savoir les reconnaitre
3- Savoir les reconnaitre
Quel que soit le sens de l’émulsion (E/H ou H/E) c’est souvent la couleur blanche qui prédomine (le lait en est le meilleur exemple d’ailleurs). Il peut être alors difficile de savoir qui est la phase continue et qui est la phase dispersée lorsqu’on regarde le liquide. Pour déterminer si l’émulsion est plutôt directe ou inverse, deux solutions peuvent être mises en place de manière relativement simple :
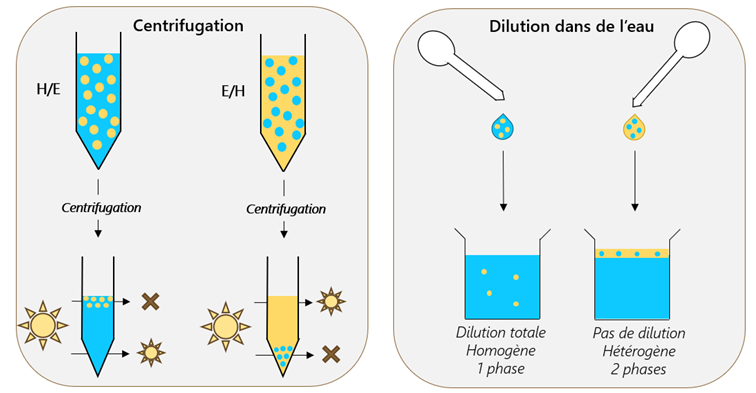
- La centrifugation : cette méthode est basée sur le fait qu’il existe un différentiel de densité entre la phase dispersée et la phase continue. Sous l’effet de la gravité, les gouttelettes vont préférentiellement se localiser en surface ou dans le fond du liquide environnant. Pour exemple, si l’émulsion est directe (phase huileuse dispersée), les gouttelettes d’huile vont se localiser plutôt en surface puisque l’huile est plus légère que l’eau. Ainsi, sous l’effet de la centrifugation, une phase dense blanche constituée des gouttes d’huile apparaitra dans le haut du tube et la phase aqueuse, située plus bas, sera quant à elle translucide. Sur les systèmes inverses, où l’eau est dispersée, les gouttelettes vont migrer vers le fond laissant alors l’huile (phase continue) sur le dessus. Que l’on se rassure, si vous ne possédez pas de centrifugeuse, laissez faire le temps, la séparation finira par se faire à condition d’être dans un liquide suffisamment fluide.
- La dilution : Si vous n’avez pas de centrifugeuse et que vous n’avez pas le temps d’attendre, alors cette méthode est tout indiquée. Il vous suffit de préparer un récipient avec de l’eau puis de prélever quelques gouttes du système émulsionné. Déposez alors le prélèvement et agitez délicatement. Ici, la méthode repose sur le fait que les émulsions possèdent la propriété de leur phase continue. Si l’émulsion est directe (H/E), alors celle-ci se diluera sans problème dans l’eau contenue dans le récipient. Si au contraire l’émulsion est inverse (E/H) alors celle-ci se retrouvera en surface de l’eau sans pouvoir se mélanger.
Conclusion
Les émulsions sont des systèmes complexes dont la formation et la stabilité sont dictés par énormément de paramètres qu’ils soient intrinsèques à la formulation (agent stabilisant, proportion des phases en présence, nature des ingrédients…) ou externes (température, cisaillement ou repos post-formation…). Les comprendre et les maitriser demande alors un certain savoir-faire. Au CRT AGIR, ces systèmes nous intéressent depuis de nombreuses années que ce soit sur des systèmes modèles ou des mises en application réelles donc si jamais vous continuez à vous interroger sur ces aspects, nous pouvons répondre à vos questions et si jamais nous n’y arrivons pas, sachez que nous aimons les défis scientifiques et technologiques.

 3- Savoir les reconnaitre
3- Savoir les reconnaitre