Le gluten est un mot dérivé du latin signifiant « colle ». Par métonymie, nous associons le gluten à la protéine du blé, mais il s’agit en réalité d’un mélange de protéines de réserve du blé ou d’autres céréales (orge, seigle, épeautre, kamut, triticale). Ce terme désigne également le réseau qu’il forme par réticulation de ces macromolécules protéiques. Aujourd’hui et malgré des décennies d’études, la compréhension du gluten reste partielle du fait de la complexité de ses interactions à multi-échelle : moléculaire, intermédiaire et macroscopique. Dans cet article, nous verrons la structure des protéines et la formation du réseau gluténique. Ensuite, nous aborderons les propriétés fonctionnelles qu’il apporte.
Structure moléculaire et formation du réseau gluténique
Classification des protéines du blé
Les protéines du blé sont classées en quatre grandes catégories selon leur solubilité dans différents solvants : les albumines, les globulines, les gliadines et les gluténines. Les albumines sont solubles dans l’eau, les globulines dans les solutions salines. Ce sont des protéines métaboliques, c’est-à-dire qu’elles participent aux fonctions vitales du grain : croissance, défense, régulation du métabolisme. Les gliadines, quant à elles, sont solubles dans les alcools dilués et les gluténines sont solubles dans les solutions acides ou basiques diluées. Ces dernières sont des protéines de réserve accumulées dans l’endosperme du grain. Elles servent de réserve d’acides aminés et d’azote pour nourrir l’embryon lors de la germination.
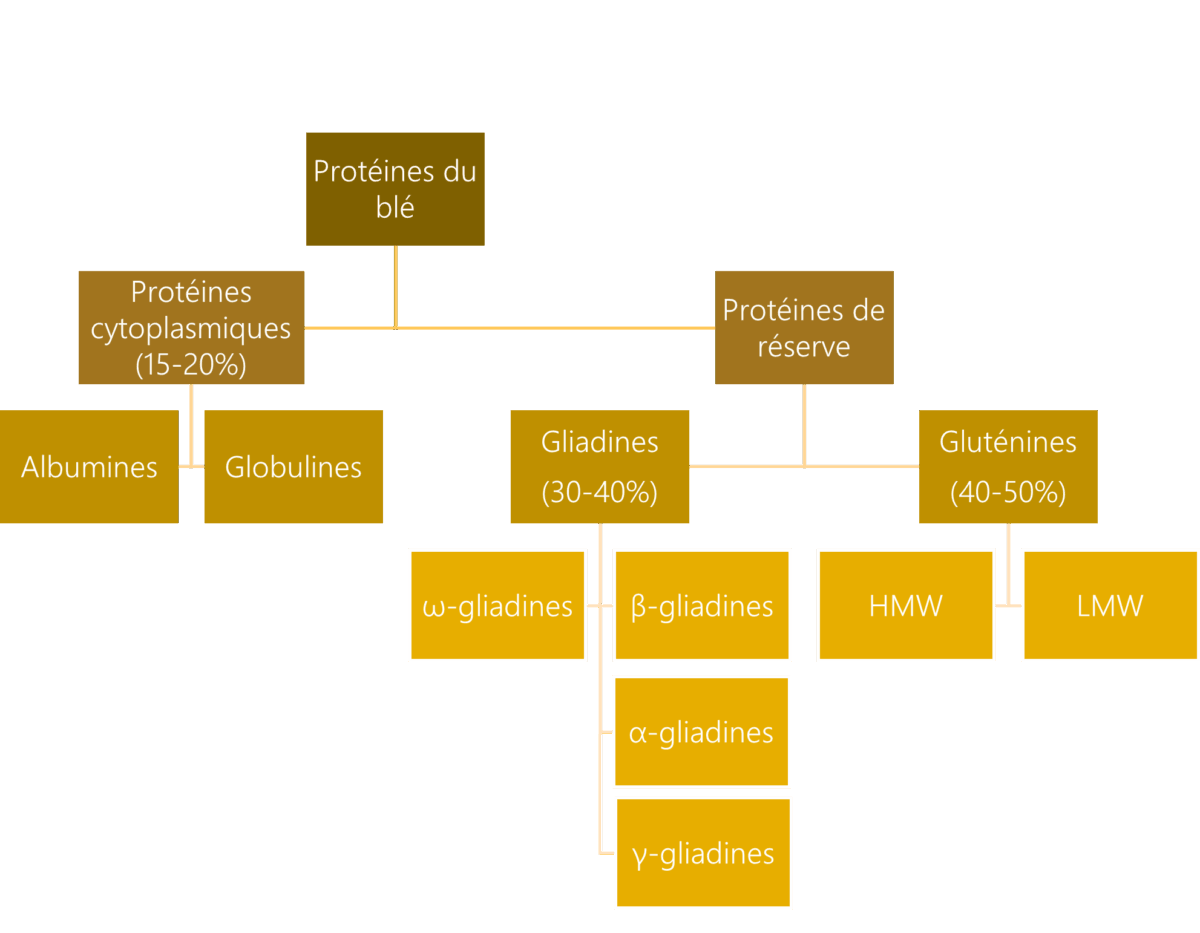
Figure 1 : Classification des protéines issues du blé (Schéma AGIR reproduit d'après Feillet, P. Le Grain de Blé)
Les gliadines représentent 30-40 % de la fraction soluble dans l’éthanol des protéines de la farine. Ce sont des protéines monomériques, constituées d’une seule chaîne, associées par des liaisons hydrogène et des interactions hydrophobes. Le poids moléculaire est compris entre 30-80 kDa. Elles sont classées en fonction de leur mobilité croissante sur électrophorèse : -ω, -γ, -β, et -α. Il est admis que les gliadines sont responsables de la composante visqueuse du comportement rhéologique des pâtes et de leur extensibilité. Les gluténines sont la fraction insoluble dans l’eau et représentent 40-50 % des protéines totales de la farine. Elles sont constituées de deux sous-unités de masse moléculaire différente : une sous-unité de faible masse moléculaire (LMW) et une sous-unité de masse moléculaire élevée (HMW). Le poids moléculaire est compris entre 500 kDa et 10 MDa. Il est admis que les gluténines sont responsables de la composante élastique et tenace des pâtes.
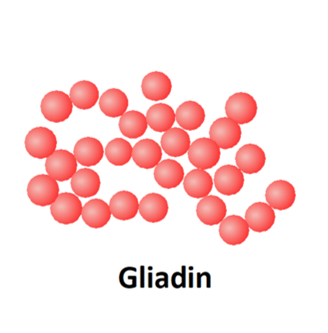
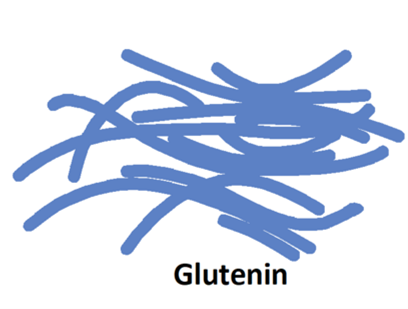
Figure 2 : Représentation schématique des protéines constitutives du gluten (gliadines et gluténines). Source : schéma adapté d'après Silva et Friscio, 2021.
Formation du réseau
La première étape correspond au mélange de l’eau et de la farine. Lors du pétrissage, l’ajout d’eau hydrate les particules de farine, ce qui accroît la mobilité de leurs chaînes moléculaires et provoque le gonflement des granules d’amidon. À la deuxième étape, en plus de l’action de l’eau, l’énergie mécanique du pétrissage provoque une redistribution des particules et conduit à la formation d’un réseau protéique viscoélastique. Le cisaillement mécanique fragmente les masses de protéines de gluten et rompt les liaisons disulfure, permettant aux molécules de gluténine de s’étirer au-delà de leur forme d’équilibre. Certaines liaisons hydrogène demeurent intactes et garantissent l’élasticité du réseau. Pendant le repos de la pâte, de nouvelles liaisons disulfure se reforment, entraînant une restructuration du réseau de gluténines. Les gliadines, quant à elles, ne participent pas directement à la formation du réseau, mais jouent un rôle de plastifiant : elles augmentent la distance entre les chaînes et équilibrent la viscosité et l’élasticité de la pâte. La troisième étape correspond au chauffage et à la stabilisation du produit cuit. Lorsque la température dépasse 60°C, l’amidon gélatinise, tandis que le réseau de gluten retient les gaz et stabilise la structure alvéolaire caractéristique de la mie du pain. Enfin, la quatrième étape correspond au refroidissement, le produit final présente des différences de teneur en eau : la mie reste humide (35 à 40 %), tandis que la croûte est beaucoup plus sèche (3 à 7 %).
Interactions moléculaires
Les protéines sont de grandes molécules formées d’acides aminés reliés entre eux par des liaisons peptidiques. Elles se replient dans l’espace pour former des structures compactes en pelotes tridimensionnelles. Les gliadines et les gluténines interagissent entre elles par la formation de liaisons covalentes et non covalentes pour former le réseau de gluten lors du pétrissage. Parmi les liaisons covalentes essentielles présentes dans ce réseau figurent les ponts disulfures (entre deux atomes de soufre). Et, des interactions non-covalentes ont également lieu telles que les liaisons hydrogène (entre régions légèrement positives et négatives), les liaisons ioniques (entre charges opposées), les interactions hydrophobes (regroupement de zones qui fuient l’eau) et les forces de Van der Waals (faible attraction entre molécules proches).
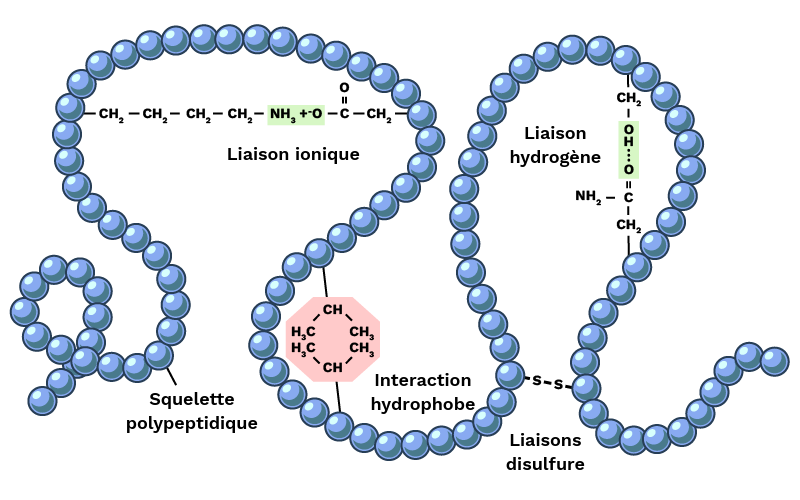
Figure 3 : Interactions impliquées dans la structuration du réseau gluténique. Source : Labster
Le gluten est donc un complexe protéique viscoélastique constitué d’un mélange hétérogène de gliadines et de gluténines associées par des liaisons covalentes, non-covalentes et des interactions hydrophobes. Ce dernier est constitué de 75-85 % de protéines, mais aussi d’un peu d'amidon (8-10 %), de sucres réducteurs (1-2 %), de lipides (5-10 %), de pentosanes (2 %) et de matières minérales (1 %).
Facteurs influençant la structure
La structure du réseau de gluten évolue tout au long de sa transformation. Les processus technologiques subis modifient la conformation des protéines et la nature de leurs interactions. Lors du pétrissage, l’action mécanique entraîne des phénomènes de dépolymérisation et de repolymérisation des protéines, à l’origine de la formation du réseau viscoélastique. On observe alors une réorganisation progressive des structures secondaires traduisant une structuration plus ordonnée.
L’hydratation joue un rôle central : en agissant comme plastifiant, elle favorise le passage de structures désordonnées vers des conformations plus organisées. Au-delà de 60 % d’humidité, les chaînes protéiques deviennent plus étendues et plus flexibles. Différentes concentrations d’eau modifient la structure du réseau de gluten :
- Une pâte contenant peu d’eau présente une structure compacte et un réseau protéique distribué de manière non-uniforme.
- Une teneur en eau intermédiaire permet d’obtenir des protéines bien réparties et orientées (par des liaisons covalentes, hydrophobes, ioniques et hydrogène).
- En revanche, une pâte contenant trop d’eau présente des protéines plus agrégées, mais moins interconnectées.
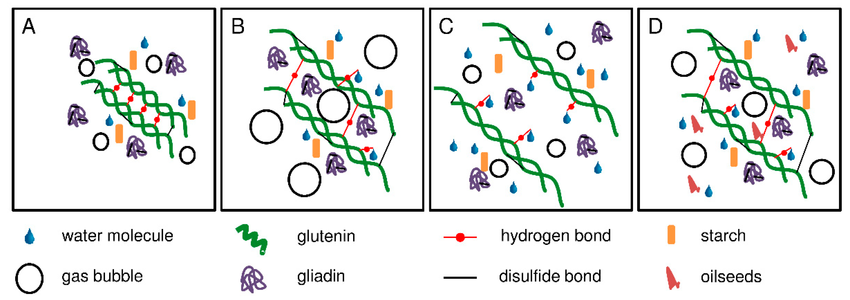
Figure 4 : Représentation schématique de la formation du réseau de gluten en fonction de la teneur en eau. (A) : farine de blé faible avec une teneur en eau inférieure à l’optimum ; (B) : farine de blé faible avec une teneur en eau optimale ; (C) : farine de blé faible avec une teneur en eau supérieure à l’optimum ; (D) : mélange pour boulangerie avec une teneur en eau optimale. Source : Schopf & Scherf, 2021.
La température du pétrissage module également ce dernier. A 30°C, les liaisons covalentes dominent, alors qu’entre 4–15°C, les interactions hydrophobes deviennent prépondérantes. Ces effets combinés de l’eau et de la chaleur déterminent l’équilibre entre élasticité et cohésion du réseau. La congélation entraîne une agrégation des protéines du gluten : avec un dépliement partiel des chaînes et la formation de liaisons hydrogène faibles. La recristallisation de l’eau perturbe sa distribution dans la pâte et les gliadines en sont particulièrement sensibles. Globalement, la congélation induit une agrégation irréversible qui altère la cohésion. Enfin, divers additifs technologiques modifient la conformation du gluten. Les sels, à faible concentration, favorisent une légère agrégation, mais à fortes doses, ils désorganisent le réseau. En panification, certains émulsifiants (Sodium stearoyl-2-lactylate E481, esters mono- et diacétyltartriques de mono- et diglycérides E472e) à faible concentration, produisent un réseau plus homogène et souple, mais à forte dose, induisent un désordre structurel.
Propriétés fonctionnelles et comportement en transformation
Viscosité et élasticité
L’analyse du profil de texture des pâtes céréalières montre que l’ajout de gluten influence fortement leurs propriétés physiques, notamment leur élasticité et leur résistance à la déformation. Une quantité modérée de gluten (10-20 %), renforce le réseau de protéines et stabilise la pâte à pain pendant le pétrissage. Cela améliore sa cohésion et sa résistance mécanique. En revanche, un excès de gluten (plus de 30 %) déséquilibre cette structure : la pâte devient plus fluide, collante et moins stable. En effet, l’augmentation du gluten provoque d’abord une hausse de certains paramètres rhéologiques (modules élastique (G′) et visqueux (G″)), qui traduisent une pâte plus ferme et plus résistante à la déformation. Mais lorsque la quantité de gluten devient trop élevée, ces valeurs diminuent à cause d’une absorption excessive d’eau par les protéines.
Rétention de gaz et porosité
Le réseau formé joue un rôle clé dans la capacité de la pâte à retenir les gaz pendant la fermentation et la cuisson. Les protéines s’agencent en une matrice viscoélastique capable d’emprisonner les bulles de CO₂. L’ajout de gluten entraîne une augmentation de presque 30 % du coefficient de rétention de gaz. Néanmoins, l’accumulation de CO₂ et l’expansion des bulles dégradent la microstructure gluténique, entraînant un raccourcissement des filaments protéiques du réseau et une augmentation du nombre de ruptures. La porosité des pâtes varie fortement selon la quantité de gluten ajoutée. Avec une proportion modérée (10 à 20 %), la pâte gagne en volume et présente de grands pores irréguliers, caractéristiques d’un réseau de gluten encore en formation. Pour des ajouts intermédiaires (20 à 40 %), le réseau se resserre, donnant des pores plus petits et plus denses ainsi qu’une porosité globale plus stable. En revanche, un excès de gluten (environ 50 %) fragilise la structure et augmente de nouveau la porosité.
Cohésion et résilience
L’augmentation de gluten modifie notablement les caractéristiques sensorielles de la matrice alimentaire. Elle réduit la dureté (la force nécessaire pour écraser le produit), le collant (la sensation de mie qui adhère aux dents) et la masticabilité (l’effort requis pour broyer et avaler), ce qui donne un produit plus tendre et agréable en bouche. En parallèle, l’élasticité (la capacité de la mie à reprendre sa forme après déformation), la cohésion (la capacité des particules à rester unies) et la résilience (la rapidité avec laquelle le produit retrouve sa forme initiale après compression) augmentent, reflétant une meilleure tenue de la mie.
Rassissement
Au cours du vieillissement, le pain subit un durcissement progressif de la mie, phénomène appelé rassissement, lié principalement à la restructuration de l’amidon et à la perte d’humidité. La dureté de la mie augmente donc naturellement avec le temps. Mais l’enrichissement en gluten ralentit ce durcissement et limite la dégradation de la texture, contribuant ainsi à une meilleure stabilité et qualité organoleptique du produit au cours du stockage.
Influence des paramètres procédés
Les propriétés du réseau de gluten dépendent fortement des conditions de traitement. La température influence la solubilité et l’agrégation des protéines : un chauffage modéré favorise la formation de liaisons hydrophobes et de ponts disulfures, ce qui renforce la cohésion de la pâte. Tandis qu’une température trop élevée provoque la dénaturation des protéines et fragilise le réseau. Le cisaillement mécanique du pétrissage favorise l’alignement et l’entrelacement des chaînes de gluten. Cela permet d’augmenter l’élasticité et la résistance de la pâte. Toutefois, un cisaillement excessif peut rompre ces liaisons. Le pH agit sur les charges électriques des protéines : une légère acidification peut améliorer la solubilité et l’hydratation du gluten. Mais, un pH extrême perturbe les interactions non-covalentes et déstabilise le réseau. Enfin, les enzymes, comme les protéases et transglutaminases, modifient la matrice protéique. Les protéases assouplissent la pâte en coupant les chaînes de gluten. Et les transglutaminases créent de nouvelles liaisons covalentes, renforçant la cohésion et la stabilité de la pâte. Ainsi, la maîtrise de ces paramètres est cruciale pour optimiser simultanément l’élasticité, la cohésion et la capacité de rétention de gaz de la pâte.
Conclusion
Le gluten, bien plus qu’une simple « colle », constitue le réseau protéique fonctionnel du blé. Son rôle ne se limite pas à la simple structuration : il interagit de manière dynamique avec l’amidon, les lipides et d’autres composants, modulant les propriétés finales du produit en fonction de la quantité de protéines, de l’hydratation, de la température et des procédés de transformation. Comprendre ces mécanismes est essentiel pour optimiser la qualité sensorielle des produits panifiables. Pour aller plus loin et acquérir une maîtrise pratique de ces notions, le CRT AGIR propose la formation « Du blé à la farine », dédiée à la compréhension des farines de blé et de leur transformation ainsi que leurs interactions avec les autres ingrédients présents dans les produits céréaliers, notamment sucrés.
Sources bibliographiques :
Feillet, P. Le grain de blé. 2000. Editions INRA Quae. https://www.quae.com/produit/437/9782759212811/le-grain-de-ble
Silva, N.A.; Friscio, F.C. A química do pão de fermentação natural e as transformações na nossa relação com o preparo desse alimento. Quimica e Sociedade 2021, Vol 43, N°3, p. 232-243, http://dx.doi.org/10.21577/0104-8899.20160239
Labster : https://theory.labster.com/fr/protein_interactions/ consulté le 05/01/2026.
Schopf, M.; Scherf, K.A. Water Absorption Capacity Determines the Functionality of Vital Gluten Related to Specific Bread Volume. Foods 2021, 10, 228. https://doi.org/10.3390/foods10020228

